
AG Bröring
Prof. Dr. rer. nat. Ruth Bröring
Medizinisches Forschungszentrum,
Gastro MFZ, 1. OG
Chronische Lebererkrankungen werden durch kontinuierliche oder wiederholte Schädigung der Leber verursacht und führen zu Fibrose und Zirrhose, die Entzündungs- bzw. Vernarbungsprozesse darstellen. Eine Vielzahl von Ursachen wie Virusinfektionen, Toxinexposition, Alkoholmissbrauch, Stoffwechsel- und genetische Erkrankungen werden mit anhaltenden Leberschäden in Verbindung gebracht und bergen ein Risiko für die Entstehung hepatozellulärer Karzinome.
Unser Team hat eine All-in-One-Technik zur Präparation von Leberzellen aus menschlichem Gewebe entwickelt, die die Analyse zelltypspezifischer, leberspezifischer und krankheitsspezifischer Aspekte auf zellulärer und molekularer Ebene ermöglicht. Die parenchymalen und nicht-parenchymalen Zellen der Leber sind Teil des angeborenen Immunsystems. Sie exprimieren evolutionär hoch konservierte, vererbbare Faktoren, die so genannten Pathogenerkennungsrezeptoren (PRRs).
Sie detektieren molekulare Strukturen von Viren, Bakterien, Pilzen und Parasiten, die in höheren Organismen nicht vorkommen. Es werden aber auch schadenassoziierte molekulare Muster erkannt, was auf eine bedeutende Rolle bei chronischer Leberschädigung deutet. Die PRRs stellen eine der ersten Verteidigungslinien gegen eindringende Krankheitserreger dar und vermitteln durch die Expression von entzündlichen Zytokinen, antiviralen Faktoren und chemotaktischen Substanzen eine koordinierte Immunantwort. Ein krankheitsbedingtes Ungleichgewicht des hepatischen Immunsystems hat Auswirkungen auf I) Wachstum und Regeneration, die durch den Hippo-Signalweg kontrolliert werden, II) Funktionen des endoplasmatischen Retikulums und des Golgi-Apparates und III) Authophagie und intrazelluläre Transportprozesse. Das Hauptziel der Forschung besteht darin, die pathophysiologischen Prozesse auf molekularer Ebene aufzudecken, um den Verlauf chronischer Lebererkrankungen zu überwachen und Therapien zu verbessern.
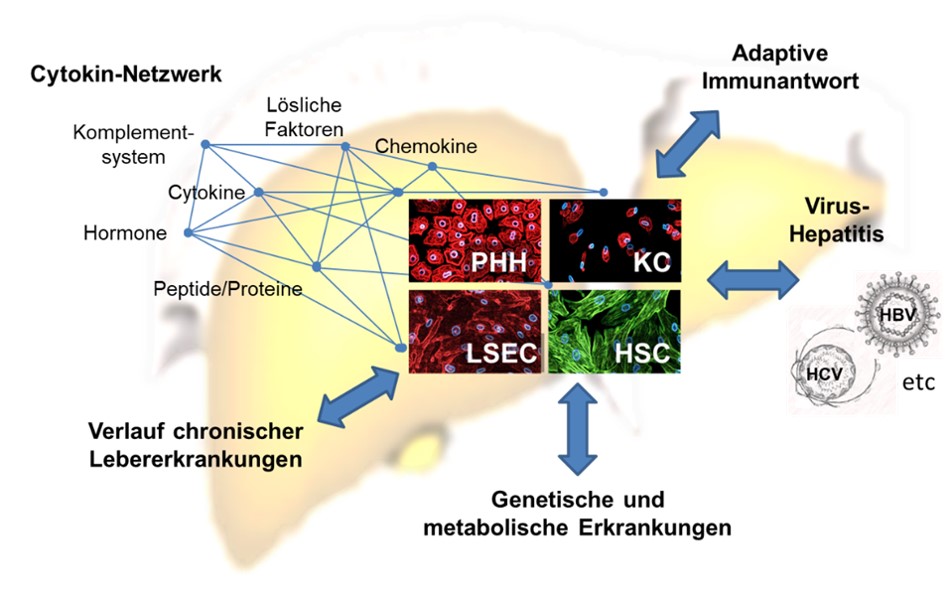
… den Einfluss parenchymaler und nicht-parenchymaler Leberzellen auf die Hepatitis-B-Virusinfektion und inwiefern Virus-Wirt-Interaktionen Immunpathologie und Chronizität bestimmen.
… die Rolle der HBe- und HBs-Antigene bei der Umgehung endogener angeborener Immunantworten anhand von Modellen zur Hepatitis-B-Virusinfektion.
… wie das HBs-Antigen Stress im endoplasmatischen Retikulum induziert, Autophagie Prozesse beeinträchtigt und Proliferation sowie Hepatokarzinogenese fördert.
… multimolekulare Therapie-Strategien gegen Kupferüberladung bei Morbus Wilson (WilsonMed).
… die Auswirkungen der Wilson-Krankheit auf die angeborene Signalübertragung, die Aktivität des Hippo-Wegs und den intrazellulären Transport im Zellkulturmodell.
- Luo X, Zhang R, Schefczyk S, Liang Y, Lin SS, Liu S, Baba HA, Lange CM, Wedemeyer H, Lu M, Broering R. Nuclear translocation of YAP drives BMI1-associated hepatocarcinogenesis in hepatitis B virus infection. Liver Int. 2023 Jun 14. doi: 10.1111/liv.15628. Online ahead of print.
- Schrader JA, Burkard TL, Brüggemann Y, Gömer A, Meister TL, Fu RM, Mehnert AK, Dao Thi VL, Behrendt P, Durantel D, Broering R, Vondran FWR, Todt D, Kinast V, Steinmann E. EGF receptor modulates HEV entry in human hepatocytes. Hepatology. 2023 Jun 1;77(6):2104-2117.
- Meister TL, Brüggemann Y, Nocke MK, Ulrich RG, Schuhenn J, Sutter K, Gömer A, Bader V, Winklhofer KF, Broering R, Verhoye L, Meuleman P, Vondran FWR, Camuzet C, Cocquerel L, Todt D, Steinmann E. A ribavirin-induced ORF2 single-nucleotide variant produces defective hepatitis E virus particles with immune decoy function. Proc Natl Acad Sci U S A. 2022 Aug 23;119(34):e2202653119.
- Werner M, Schefczyk S, Trippler M, Treckmann JW, Baba HA, Gerken G, Schlaak JF, Broering R. Antiviral toll-like receptor signaling in non-parenchymal liver cells is restricted to TLR3. Viruses 2022, 14(2), 218.
- Luo X, Zhang R, Lu M, Liu S, Baba HA, Gerken G, Wedemeyer H, Broering R. Hippo pathway counter-regulates innate immunity in Hepatitis B virus infection. Front Immunol. 2021 May 25;12:684424.
- Du Y, Anastasiou OE, Strunz B, Scheuten J, Bremer B, Kraft A, Kleinsimglinhaus K, Todt D, Broering R, Hardtke-Wolenski M, Wu J, Yang D, Dittmer U, Lu M, Cornberg M, Björkström NK, Khera T, Wedemeyer H. The impact of hepatitis B surface antigen on natural killer cells in patients with chronic hepatitis B infection. Liver Int. 2021 Sep;41(9):2046-2058.
- Zhou L, He R, Fang P, Li M, Yu H, Wang Q, Yi Y, Wang F, Zhang Y, Chen A, Peng N, Lin Y, Zhang R, Trilling M, Broering R, Lu M, Zhu Y, Liu S. Hepatitis B Virus rigs the cellular metabolome to avoid innate immune recognition. Nat Commun. 2021 Jan 4;12(1):98.
- Kinast V, Plociennikowska A, Anggakusuma, Bracht T, Todt D, Brown RJP, Boldanova T, Zhang Y, Brüggemann Y, Friesland M, Engelmann M, Vieyres G, Broering R, Vondran FWR, Heim MH, Sitek B, Bartenschlager R, Pietschmann T, Steinmann E. C19orf66 is an interferon-induced inhibitor of HCV replication restricting formation of the viral replication organelle. J Hepatol. 2020 Sep;73(3):549-558.
- Zhang Z, Trippler M, Real CI, Werner M, Luo X, Schefczyk S, Kemper T, Anastasiou OE, Ladiges Y, Treckmann J, Paul A, Baba HA, Allweiss L, Dandri M, Gerken G, Wedemeyer H, Schlaak JF, Lu M, Broering R. Hepatitis B Virus Particles Activate Toll-Like Receptor 2 Signaling Initially Upon Infection of Primary Human Hepatocytes. Hepatology. 2020 Sep;72(3):829-844.
- Yu H, Li M, He R, Fang P, Wang Q, Yi Y, Wang F, Zhou L, Zhang Y, Chen A, Peng N, Lu M, Trilling M, Broering R, Zhu Y, Liu S. MVP promotes hepatocellular carcinoma via targeting IRF2 and decreasing p53 activity. Hepatology 2020 Aug;72(2):518-534.
Mitarbeiter

Dr. rer. nat.
Stefan Schefczyk
M.Sc. Biologie, AG Bröring

Caini Yang
cand. Dr. med., Doktorandin, AG Bröring

Martha-Julia Sasula
M. Sc. Molekulare Zellbiologie, AG Bröring

Lorraine Tendai Muungani
M.Sc. Biologie, AG Bröring

Anna Held
cand. Dr. med., Doktorandin, AG Bröring

Prof. Dr. rer. nat.
Ruth Bröring
Diplom Biologin, Laborleitung
